数字化转型与质量管理数字化有什么联系?

随着2019年新《药品管理法》出台,新形势下GMP合规也在蜕变,我们不难感受到两个很明显的变化,一是取消GMP认证证书取而代之的是GMP合规检查;二是GMP检查制度和监管理念也在向FDA接轨靠拢。那么未来中国药企自己的质量管理应该朝什么方向去改变?我们不仅要看中国目前监管的要求,同时还要看国际上,尤其是FDA监管思路的变化,这样我们才能提前做好充分的准备工作。
一、质量合规性的产业发展趋势
经过近10年的行业产业发展和轻工业4.0黄金时代的来临,许多大型药企早已从最基础如前所述信用风险的市场监管和质量管理,进入了质量管理4.0黄金时代。我们可以显著看到的一个趋势是药企导入更多数字化的远距工具来协助质量管理体系稳步提高。同样,市场监管政府机构也在逐步使用数字化的市场监管方式来远距进行数据分析和信息市场监管。数字化的质量控制系统在借力药企的与此同时,还能进一步推动质量量测和质量管理适用性的提高,协助药企稳步改良,达到控制系统助推合规性的效果。
二、生物科技行业数字化格局
领跑的生物科技企业早已在积极借助于数字化远距工具给各个业务模块借力,相信大家对经营管理、研制、生产、仓储板块的软件控制系统都不孤单,但对质量数字化控制系统因为其合规性市场监管严格、法律法规信用风险高等行业技术壁垒,目前对许多生物科技企业而言还是处于起跑阶段。但在近在咫尺的将来,随著行业法律法规的逐步完善和对数据完备性的重视,和轻工业4.0质量管理控制系统在生产制造端进一步根植破冰,整个质量管理必须要能渗入研制生产仓储的根源,由此看来质量管理的数字化基本难成毋庸之势。我们极难想像在轻工业4.0或智能化制造2025充份展开的与此同时,药企还会存在着一套实体店的纸本的质量管理体系。
三、既然药企的质量管理数字化已是毋庸之势,所以我们该怎样开展工作?
1、对大多数生物科技企业而言,优先选择一个专精的数字化质量管理软件系统服务商,充份运用分销商的专精能力是一个不错的优先选择。所以,要怎样就可以优先选择到最合适的质量管理控制系统呢?
(1)GMP全球合规性:能保证计算机控制系统符合GMP合规性性管理水平,能满足FDA、欧洲联盟审计工作明确要求。经得住国内外非官方市场监管政府机构的检查和合格证书、和客户的分销商审计工作;
(2)先进的IT技术构架和高可配置能力:控制系统是如前所述新一代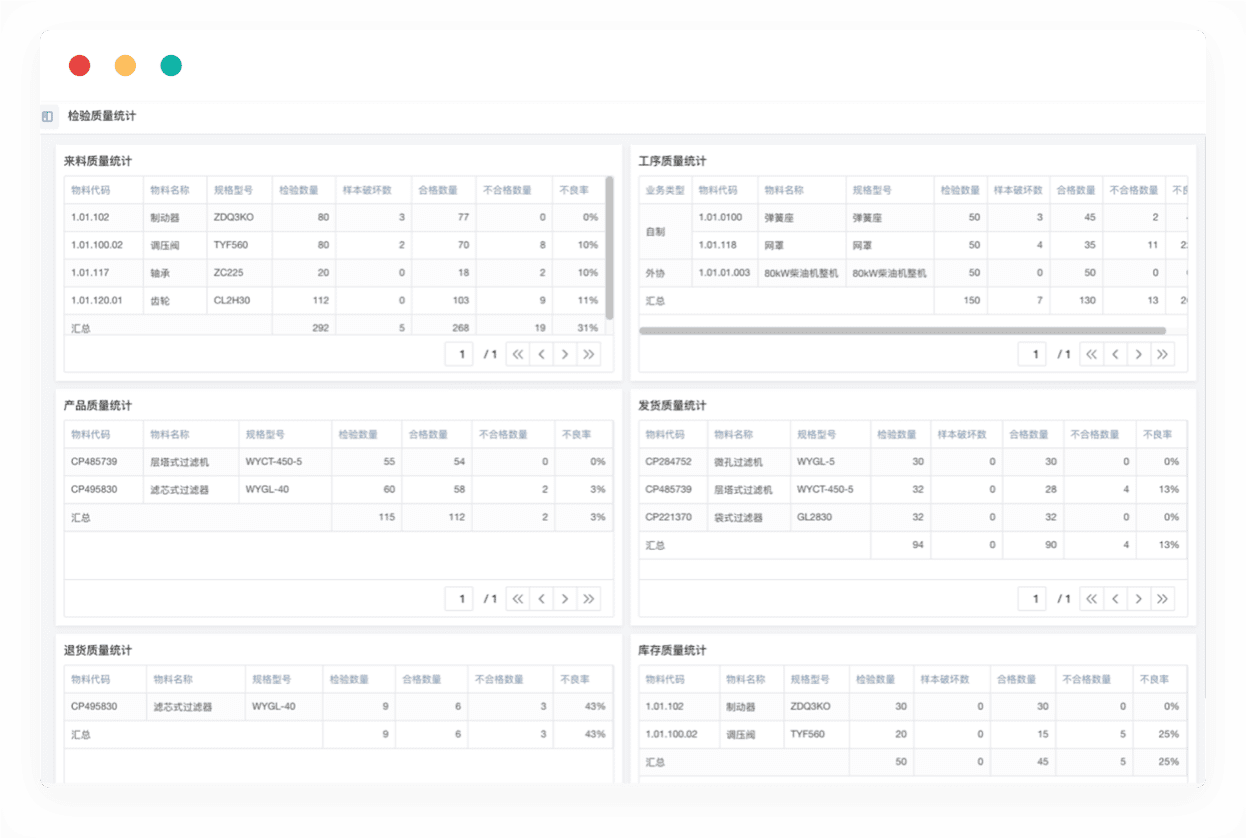 信息技术而不是老的技术,可以显著降低拥有成本并提高效率;可以在不进行定制开发的情况下满足企业质量管理管理体系稳步升级进化的需求,在降低验证成本的与此同时,避免国内大部分软件通过定制开发实现业务需求的质量信用风险和合规性性信用风险;
信息技术而不是老的技术,可以显著降低拥有成本并提高效率;可以在不进行定制开发的情况下满足企业质量管理管理体系稳步升级进化的需求,在降低验证成本的与此同时,避免国内大部分软件通过定制开发实现业务需求的质量信用风险和合规性性信用风险;
(3)良好的产品交互设计和用户体验:界面容易理解,符合中国人的操作习惯,几乎不需要培训就能使用,使用起来高效便捷;质量管理控制系统
2、当我们在选型质量管理控制系统eGMP(QMS、DMS、TMS)时,怎样在市场上琳琅满目的软件产品中保证你找到的是最最合适的控制系统呢?
正所谓,百闻不如一见,百见不如一试!正确的姿势是试用、试用、还是试用!一个真正好的产品,一定是经得住试用的,在试用的过程中您可以了解该软件产品全面的功能、整体的可用性和企业自身的适用性接受程度等等,可以充份了解软件产品涵盖的实施范围,并对技术支持展开彻底的评估和判断;除了考量控制系统外,试用也是双方共同参与项目的真实缩影,从中更好了解彼此,确认项目的现实期望,排除未知消除疑虑,达成共识,建立互信,为日后正式合作奠定良好基础。
最后,推荐一款非常好用的质量管理控制系统。简道云质量管理控制系统致力于解决制造业质检效率低下、作业不规范等各种难题,有效为企业质量管理提速降本。该控制系统能有效提高质检沟通效率,降低质量试错成本,加快数据统计速度,如前所述无编程平台简道云,搭建「质量管理应用」,形成质量检验、质量方案、档案数据、统计分析一体化的质量管理管理体系。